vol.1
COVID-19の治療薬候補を
既存薬の中から計算で探し出す

私たちの生活を一変させた新型コロナウイルス感染症(COVID-19)。世界中の製薬会社や研究機関がその治療薬の開発に取り組んでいます。奥野さんは、スーパーコンピュータ「富岳」を中核とするHPCI(革新的ハイパフォーマンス・コンピューティング・インフラ)を利用して精密なシミュレーションを行い、2128種類もの既存薬(すでに他の病気の治療に使われている薬)の中からCOVID-19の治療薬として有望な候補を見つけることに成功しました。

精密なシミュレーションから生まれた「驚くほどよい結果」
COVID-19の被害を抑え、経済・社会活動を回復するために、治療薬やワクチンの開発が急ピッチで進められています。治療薬については、抗ウイルス薬を中心とした既存薬の中から新型コロナウイルスに効果を示すものを見つけ出そうという動きがさかんです。既存薬は治験で安全性が確認されているため、開発期間の短縮が期待できるからです。しかし、世界中で細胞実験から治験まで様々なレベルの研究が行われているにもかかわらず、まだ効果的な治療薬の発見には至っていません。
こうした状況の中、期待を集めているのがスーパーコンピュータを活用したシミュレーションです。「実験よりもずっと短い時間でたくさんの薬を調べることができる上に、薬の作用の仕方までわかるからです」と奥野さんは説明します。奥野さんは、理化学研究所などが開発・整備中の新型コロナウイルス対策のための「富岳」の優先的な試行的利用と、HPCIコロナウイルス感染症対応臨時公募を利用し、「富岳」と、筑波大学の「Cygnus」を使って、2020年4月に既存薬の中からCOVID-19の治療薬候補を探索する研究に着手しました。
「富岳」を用いた研究課題は、新型コロナウイルスが細胞内で増殖する際に重要な「メインプロテアーゼ(NSP5)」というタンパク質をターゲットとし、2128種類もの既存薬の中から治療薬の候補を探そうというものです。「富岳」の中にこのタンパク質と既存薬分子のモデルをつくり、「分子動力学シミュレーション」という手法でタンパク質と薬分子のふるまいを計算しました。「この計算により、タンパク質の活性ポケット*1が開いたり閉じたりする様子や、薬分子が離れたところからやってきて活性ポケットや他の部分にくっついたり離れたりする様子を、精密に再現することができました(図1)」。
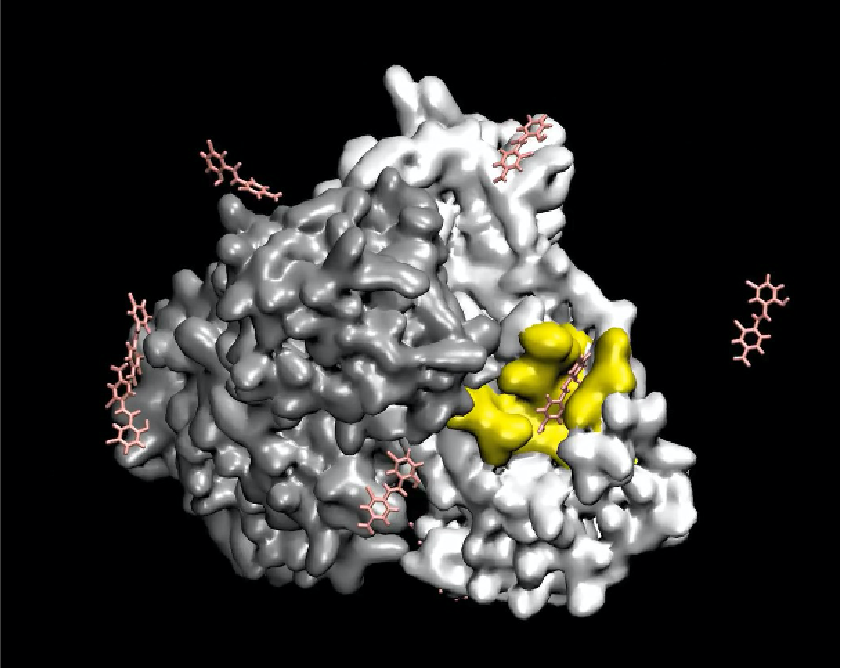
図1
「富岳」で行った分子動力学シミュレーションの一例
新型コロナウイルスの増殖に重要なメインプロテアーゼというタンパク質(灰色)と、ニクロサミドという既存薬(ピンク)のふるまいをシミュレーションした動画の一場面。活性ポケット(黄色)に1個の薬分子が入り込んでおり、タンパク質から離れている薬分子や、活性ポケットとは別の場所にくっついている薬分子もある。このようなシミュレーションを2128種の既存薬について行った。
そして、薬分子がメインプロテアーゼの活性ポケットに滞在している時間などを指標として既存薬をふるいにかけることで、数十種類の候補を選び出すことに成功しました(図2)。「これらの薬は、メインプロテアーゼに結合する能力が高いと予想され、新型コロナウイルスに薬効を示す可能性があります。シミュレーションを行う前は、このような薬がほとんど見つからないとか、逆に、たくさん見つかりすぎてしまうことを心配していましたが、妥当な数の候補が見つかりました。さらに、このうちの12種類は海外で新型コロナウイルス治療への臨床研究や治験が行われています。自分でも驚くほど、よい結果が出ました」と奥野さん。臨床研究や治験に進んだ薬は効果が確認されているわけですから、そうした薬がシミュレーションでも候補に選ばれたということは、シミュレーションの信頼性の高さを示しています。
12種類の中でも特に結合能力が高いと予想された「ニクロサミド」という薬は、日本では未承認ですが、海外では寄生虫の駆除薬として使われており、安価で安全性も確認されています。今回の結果を受けて、臨床研究に弾みがつくことが期待されます。
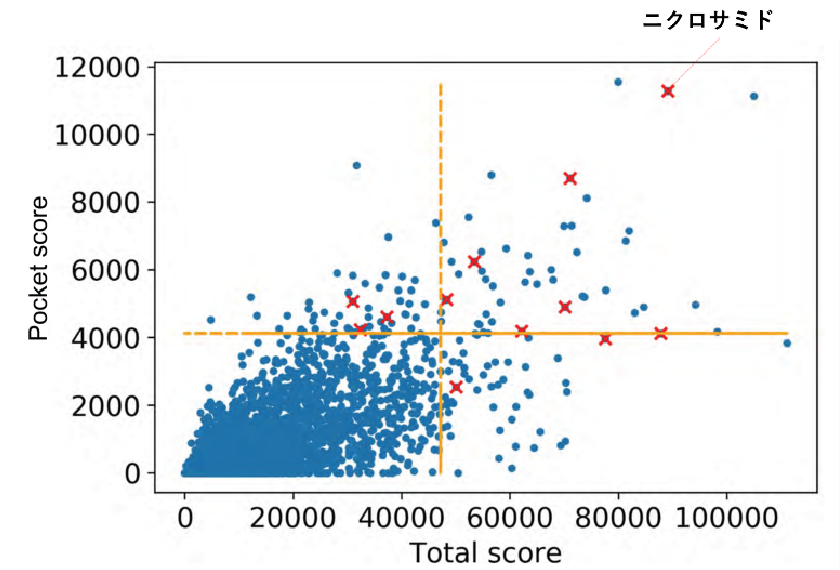
図2
治療薬候補の絞り込み
図1のようなシミュレーションで、薬がタンパク質の活性ポケットに滞在する時間(縦軸)と、タンパク質の表面のどこかに滞在する時間(横軸)を調べた。グラフ上の1個の点が、1種類の薬を表し、×は海外で臨床試験または治験が行われている薬を示す。このグラフでは右上ほどタンパク質との結合能力が高いと予測され、黄色い線で区切った右上の部分にある数十種類の薬を、治療薬の候補と判定した。
計算法の工夫で「富岳」の計算能力を生かす
奥野さんたちが「富岳」での計算を開始したのは4月末。準備期間は1ヵ月もありませんでしたが、計算は順調に進み、6月末には治療薬候補を得ることができました。こんな離れ業ができたのは、「「京」で培ったノウハウがあった上に、「富岳」がとても使いやすい計算機だったからです」。
奥野さんたちは、「京」でも薬の候補を選ぶためのシミュレーションを行っていましたが、「京」の計算能力では、今回のような精密なシミュレーションを行う場合、調べられる薬の数は数十種類ほどでした。「創薬の最初の段階では『多数の中から選ぶ』ことが重要であり、実験では非常に多くの候補を調べるのですが、「京」ではまだそのプロセスをシミュレーションで実践するには届いていませんでした。しかし、今回、「富岳」で2000種類以上の薬を計算できたことで、実践に大きく近づいたと思います」。精密な分子動力学シミュレーションにより2000種類以上の既存薬の中から候補を選び出せたことは、世界初の成果であり、計算技術としても、学術的にも大きな意義をもっています。しかも、この計算は、「富岳」のごく一部である5500ノードを使用しただけで達成されたのです。
この成功の背景には、「富岳」の計算能力に加えて、計算上の工夫や努力がいくつもありました。その1つは、計算の際に薬分子の濃度を通常の数百倍に高め、タンパク質との相互作用が起こりやすいようにしたことです。計算時間を短縮するための工夫ですが、濃度が高すぎるなど条件によっては計算ができなくなってしまうため、慎重な条件設定が必要でした。また、薬が活性ポケットに滞在する時間が実験値と整合するかも確かめました。さらに、「富岳」では膨大な計算結果が得られるため、その解析方法も同時に開発する必要がありました。
Cygnusのよさを生かして別のタンパク質もシミュレーション
筑波大学の「Cygnus」では、「富岳」で選び出された治療薬候補が、新型コロナウイルスがつくる別のタンパク質(NSP16)に結合するかどうかを調べました。NSP16の阻害剤(NSP16に結合して、その働きを抑える薬)は、メインプロテアーゼの阻害剤に比べると開発途上であり、既存薬の可能性をシミュレーションで探ることは挑戦的な試みです。
「Cygnus」は、人工知能の研究でもよく使われるGPU*2の最新版を豊富に搭載しており、分子動力学シミュレーションを高速に行うことが可能です。「『Cygnus』はすでに正式運用中でしたので、計算に取りかかるまでに短時間で計算機に合わせた準備ができ、安定した計算ができました」。
「富岳」での計算と同様、薬分子の濃度を高めて分子動力学シミュレーションを行い(図3)、その結果から、薬分子がNSP16の活性ポケットに結合する能力を予想します。計算結果は解析中ですが、タンパク質が異なれば結合しやすい薬も変わると考えられ、どのような解析結果が出るかが注目されます。
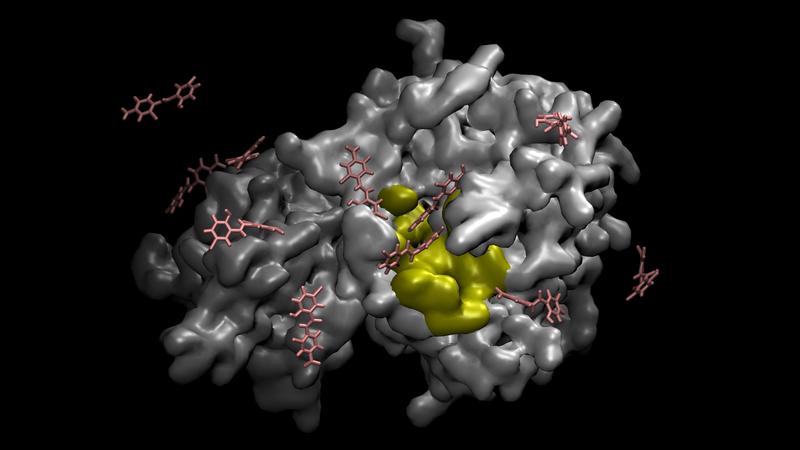
図3
Cygnusで行った分子動力学シミュレーションの一例
メインプロテアーゼをターゲットとして得られた治療薬候補であるニクロサミドと、NSP16との相互作用を、「富岳」を使用したときと同様の手法で計算した。
【用語解説 *1】
タンパク質の中には「くぼみ」をもつものがあり、そこに決まった分子が結合することで働き始める。このくぼみを「活性ポケット」と呼ぶ。決まった分子の代わりに別の分子が活性ポケットに結合すると、タンパク質の働きを抑えられる可能性があるため、そのような分子を探すことが薬の開発の第一歩となる。
戻る【用語解説 *2】
「Graphics Processing Unit」の略で、画像処理に適した演算装置を指す。コンピュータの演算装置としては、CPU(中央演算装置)が搭載される場合が多いが、計算の種類によっては、GPUのほうが計算が速い場合がある。
戻る研究者紹介

奥野さんが今回COVID-19のために用いた手法は、ほかの病気の薬の探索にも使うことができます。実際、奥野さんは、「富岳」の本格運用開始後、がんと難病の薬の候補を探索する計画です。研究にあたっては「一人ひとりのがんの違いに合った薬をすばやく選んだり、まだ薬のない難病の薬を既存薬の中から探したりするのに「富岳」の計算パワーを使えたらと考えています」と、患者さんファーストの立場を大切にしています。また、創薬のスピードを速めるために、計算機の利用だけでなく、異分野の研究者や製薬企業を巻き込んだコンソーシアムを設立するなど、精力的な活動を展開しています。目の前の患者さんに、少しでも早く薬を届けたいと願う奥野さんは、これからも計算創薬の分野を牽引し続けることでしょう。
研究課題名:
プレシジョンメディスンを加速する創薬ビッグデータ統合システムの推進(hp200129)
分子動力学計算の基づく新規作用機序を示すCOVID-19治療薬の同定(hp200155)
物理学からコンピュータへ
わたしは元々素粒子物理学が専門でしたが、実験データを分析するためにコンピュータを愛用していました。実は、物理学よりコンピュータの方が好きだったのかもしれません。当時はパソコンなどというものはなく、紙のカードにプログラムやデータをパンチして大きなコンピュータに入力していました。
1978年、運命のいたずらにより筑波大学電子・情報工学系に転任しました。
コンピュータ科学も一生懸命勉強しましたが、何か物理学とコンピュータの両方を活かすテーマがないかと漠然と考えていました。ちょうどそのころ、素粒子(陽子、中間子など)が量子色力学というゲージ理論で記述され、それを格子で近似することにより、素粒子の運動が第一原理から(つまり仮定なしに)説明できるという格子ゲージ理論が提唱されていました。
何人かの共同研究者と早速飛びついたのですが、意味のある結果を出すためには膨大な計算が必要でした。初めは大型汎用計算機を使っていましたが、1983年には日本の大学でもベクトル型のスーパーコンピュータ(スパコン)が使えるようになり、計算性能は飛躍的に増大しました。我々のグループは、高エネルギー物理学研究所(当時)のスパコンを1年に何と2000時間以上も使ってしまいました。方程式を高速に解くアルゴリズムを発明したこともあり、欧米からは、なぜ日本でこんな大きな計算ができるのか不思議がられました。
それでも、精度のよい、現実に近い結果を得るためには、さらに大規模な計算が必要となります。当時、汎用のマイクロプロセッサの性能が急速に増大し、これを多数並列に稼働させれば大規模な計算ができるようになりました。我々はこのような並列型スパコンを自主開発するプロジェクトも立ち上げました。そして市販のスパコンと自作のスパコンの両方を使って格子ゲージ理論の計算を行い、多くの成果を上げました。自主開発は大変でしたが、ほどなく日本でも商用の並列型スパコンが登場しました。現在、「京」から「富岳」へと日本の並列型スパコンが大活躍していますが、我々の苦労がけして無駄でなかったと確信しています。
次回は産官学にわたって計算物質科学の発展に尽くしておられる伊藤聡氏(FOCUS)につなぎます。伊藤氏が東芝におられた2000年代初めから、次世代スーパーコンピュータ「京」の建設や利用に向けてともに頑張ってきました。

筑波大学で共同開発した並列スーパーコンピュータCP-PACSのパネルの前で筆者

